شاید واژه ظرفیت گرمایی در جایی به چشم شما هم خورده باشد اما ندانید که این مفهوم به چه معناست.
برای هر مهندس لازم است این مفهوم مهم و کاربردی در مورد مواد مختلف را بداند.
در این مقاله سعی داریم با این مفهوم به زبان ساده آشنا می شویم.
1# مفهوم ظرفیت گرمایی
 |
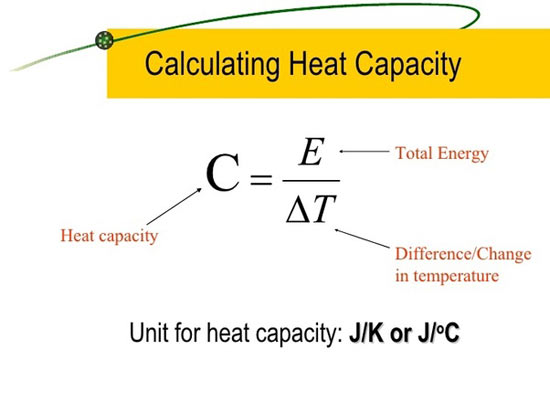
مفهوم ظرفیت گرمایی یا ظرفیت حرارتی این است که
بین گرمای مبادله شده و تغییر دمایی که از این تبادل حرارت ایجاد می شود نسبتی وجود دارد.
از مفهوم ظرفیت گرمایی در شرایطی استفاده می شود که
تبادل حرارتی که با سیستم صورت می پذیرد بتواند در آن تغییر دما را به وجود آورد اما در مواقعی که فاز تغییر می کند کارآیی ندارد.
از طرفی ظرفیت گرمایی ویژه، میزان حرارتی است به واحد جرم سیستم اعمال می شود تا
بتواند میزان دما را یک درجه سانتی گراد دچار تغییر نماید و
برای مواد به این صورت تعریف می شود که
میزان انرژی ای است که هر گرم از ماده می تواند دریافت نماید تا باعث بالاتر رفتن میزان درجه گرمای آن ماده تا حد یک درجه سانتی گراد شود.
لازم است بدانید که ظرفیت گرمایی یک ماده با گرمای ویژه آن یکسان نیست و
به عواملی مانند دما و فشار وابسته است.
هنگامی که ماده ای در حالت جامد و یا مایع گرما می بیند این امکان وجود دارد که
دمای آن افزایش نیافته بلکه از حالتی به حالت دیگر تغییر یابد به عنوان مثال از مایع به گاز تبدیل شود از همین روست که
با دریافت گرما یخ بدون آن که تغییری در دمایش ایجاد شود ذوب شده و یا آب به جوش می آید.
2# بررسی ظرفیت حرارتی گاز ها
با گرم کردن گاز، در آن انرژی جذب می شود و انرژی انتقالی آن افزایش می یابد.
این موضوع در خصوص گازهای چند اتمی باعث می شود که انرژی ارتعاشی و چرخشی افزایش یابد.
به طور کلی می توان بیان کرد که گرمای ویژه در هر دما شامل تجمیع حرارت و
گرماهای انتقالی، چرخشی، جنبشی و ارتعاشی است.
در خصوص گازهای تک اتمی، ظرفیت گرمایی مطابق با تجربیات بدست آمده در فشار مشخصی برابر 20.79 می باشد که
گرمای ویژه مربوط به گازهای تک اتمی مربوط به انرژی انتقالی جنبشی می باشد.
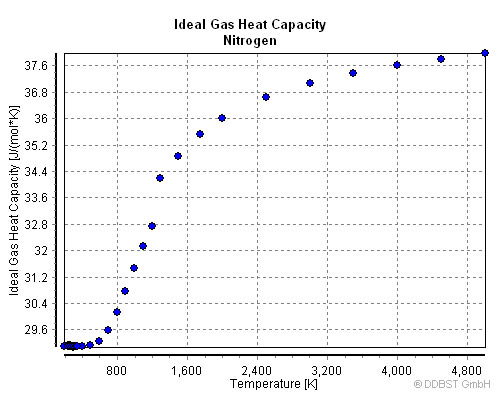
اما در مورد گازهای دو اتمی می توان گفت که دارای سه درجه آزادی انتقالی بوده و
همچنین از دو درجه آزادی چرخشی نیز برخوردار می باشد که
در دمای معمولی ظرفیت گرمایی 29.288 خواهد بود اما اگر دما زیاد باشد با در نظر گرفتن انرژی چرخشی این میزان به 37.656 خواهد رسید.
لازم به ذکر است که اندازه شدت برانگیخته شدن مولکول به عواملی همچون جرم اتمی و مستحکم بودن پیوند اتمی وابسته می باشد.
از طرفی وقتی ظرفیت گرمایی گازهای چند اتمی مطرح است،
با خطی بودن ساختار مولکولی، پنج درجه آزادی جهت انرژی های انتقالی، جنبشی و چرخشی به وجود می آید و
در خصوص درجه آزادی انرژی ارتعاشی میزان بسیار اندک است.
3# ظرفیت حرارتی جامدات
تحقیقات و آزمایشات زیادی در خصوص ظرفیت گرمایی جامدها انجام شده است.
دانشمندانی همچون دولن و پتی در اوایل سال 1800 به شکلی تجربی متوجه شدند میزان ظرفیت گرمای عنصرها در زمانی که فشار یک اتمسفر بوده و
دما معمولی است، 6.2 می باشد.
وقتی مواد به شکل جامد هستند اتم ها به شکل شبکه بلوری هستند و
حرکت های چرخشی و انتقالی ندارند و فقط حالت ارتعاشی دارند.

دانشمندان دیگری در شرایط مشابه به عدد 5.9 رسیدند در همان ابتدا
قانونی که دولن و پتی مطرح کردند در نقطه توجه قرار داشت و
می توانست نقش موثری در مشخص شدن جرم اتمی جامدات داشته باشد.
اما ادامه تحقیقات نشان داد این قواعد در خصوص عناصر سنگین و در دمای معمولی صدق می کند.
به جهت آن که قانون مذکور، ظرفیت گرمایی را جدا از دما متصور می شد.
در حالی که تابعی از دما است.
با ظهور کوانتومی بودن انرژی و رشد علم مکانیک کوانتوم، این امکان ایجاد شدن که
بر اساس نتایج تجربی انجام شده به تعابیر جدید دست یابند.
یکی دیگر از دانشمندانی که در این خصوص مطالعه می کرد بیان داشت که
ظرفیت گرمایی در شرایط صفر مطلق، به صفر نزدیک شده و یا به شدت کوچک خواهد بود.
4# بررسی ظرفیت گرمایی آب
خوب است بدانید که در دمای اتاق ظرفیت گرمایی آب در حالت یخ 37.40 ژول بر مول بوده و
در شرایط مایع به 75.38 ژول بر مول و
در شرایط بخار 36.80 ژول بر مول خواهد بود که
این موضوع کاملا به حالت فیزیکی وابسته می باشد.

حال ببینیم این تفاوت ها برای چیست؟
با مقایسه کردن ظرفیت گرمایی مولی آب در حالت های مایع و جامد می توان دریافت که
دلیل اختلافات در درجات آزادی است.
به دلیل آن که درجه آزادی در جامد نسبت به مایع کمتر است.
بنابر این ظرفیت گرمایی پایین تری نیز دارد.
اما با بررسی بیشتر می توان دریافت که تفاوت ها در تشکیل پیوند های هیدروژنی در مولکول آب، در زمانی که در حالت مایع قرار دارد می باشد.
این موضوع در مقایسه ظرفیت حرارتی آب در حالت بخار و جامد نیز صدق می کند و
می تواند به تشکیل شدن پیوند هیدروژنی مرتبط باشد.
5# دلایل تفاوت ظرفیت حرارتی آب در سه حالت مختلف
از عوامل مهم و موثر در ظرفیت گرمایی، می تواند نیروی جاذبه ای باشد که بین مولکول های یک ماده وجود دارد.
در صورتی که میزان این نیرو در میان مولکول ها زیاد باشد، جهت بالا بردن حرکت جنبشی مولکول ها می بایست گرمای زیادتری ایجاد شود و
در نهایت میزان ظرفیت گرمایی نیز افزایش می یابد.
همچنین درجات آزادی که در ماده وجود دارد و
حرکت هایی که ذرات ماده می توانند داشته باشند، در میزان ظرفیت گرمایی آن تاثیر گذار است که
این حرکات می تواند شامل حرکت های چرخشی، انتقالی و ارتعاشی باشد.
به عبارتی هر چقدر میزان آزادی ماده ای افزایش یابد ظرفیت گرمایی آن نیز بیشتر خواهد شد.
به همین دلیل است که باید جهت تعیین و توضیح ظرفیت گرمایی یک ماده به دو عامل در آن توجه نمود.
این کاملا روشن است که در حالت های آب و یخ، جاذبه بین مولکولی میزان نیرویی یکسان دارد اما
از آن جایی که درجه آزادی یخ نسبت به آب کمتر است بنابراین میزان ظرفیت گرمایی آن نیز در مقایسه با آب کمتر بوده و
تقریبا یک دوم آب می باشد.
نظرتون درباره این مقاله چیه؟
ما رو راهنمایی کنید تا اون رو کامل تر کنیم و نواقصش رو رفع کنیم.
توی بخش دیدگاه ها منتظر پیشنهادهای فوق العاده شما هستیم.


