حتما شما هم شنیده اید که قانون بقای جرم یکی از مهم ترین و پایه ای ترین قوانین کشف شده درون طبیعت است.
کاربردهای این قانون را در مکان مختلفی می توان مشاهده کرد.
این قانون چه جاهایی معتبر است و چگونه می توان درستی آن را تحقیق کرد؟
با ادامه مقاله همراه باشید تا درباره این قانون و چیستی آن بدانید.
1# قانون بقای جرم چیست؟ (Law Of Conservation Of Mass)
قانون بقای جرم بیان می دارد که جرم کل در یک سیستم ایزوله (سیستمی که تبادل ماده یا انرژی با محیط بیرون ندارد) نه از بین می رود و نه تولید می شود (نه به واسطه واکنش های شیمیایی و نه تبدیلات فیزیکی).
این قانون، کشفی از آنتوان لاوازیه (Antoine Lavoisier) در سال 1978 میلادی است و با وجود این که ما می دانیم معمولا سیستم ایزوله وجود ندارد، می توانیم خودمان محدوده ای را به عنوان سیستم ایزوله تعریف کنیم.

قانون بقای جرم در علوم مختلف به شیوه های مختلفی مطرح می شود که در ادامه می خوانید.
1-1# علم شیمی
در طی انجام یک واکنش شیمیایی، تعدادی واکنش دهنده به فرآورده تبدیل می شود.
طبق قانون بقای جرم، جرم یا تعداد اتم های واکنش دهنده ها با فرآورده ها برابر است.
اتم ها ممکن است به شکل های مختلفی تبدیل شوند؛ اما تولید یا نابود نمی شوند.
مثلا اتم های عنصری مثل کربن که در محیط زیست بسیار مهم است،
بارها در طبیعت به اشکال مختلفی در آمده است (یک واکنش سوختن را در نظر بگیرید که در آن کربن (ذغال) پس از سوختن به شکل کربن دی اکسید در می آید).
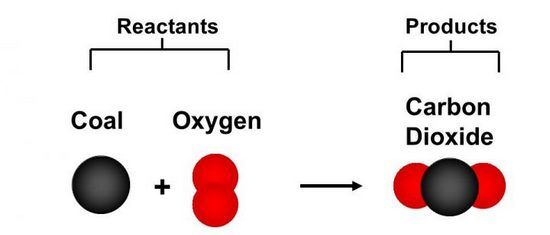
یکی از کاربردهای این قانون این است که مقدار گاز تولید شده را می توان محاسبه کرد.
در واقع می توان جرم مایعات و جامدات را اندازه گیری یا محاسبه کرد و
در صورت برابر نبودن جرم ها، می توان گفت که واکنش دهنده یا فرآورده گازی هم داریم.
2-1# علم فیزیک
در علم فیزیک قانون بقای جرم بیان های متفاوتی دارد.
مثلا در مکانیک سیالات (با استفاده از معادله پیوستگی)، این قانون به صورت فرمول زیر بیان می شود:
Dρ⁄Dt + ρ ∇. v = 0
که در آن ρ نماد چگالی، t نماد زمان و v بردار سرعت فلو است.
در سیال تراکم ناپذیر شرط زیر برقرار است:
v = 0.∇
بنابراین معادله بقا به شکل زیر خلاصه می شود:
Dρ/Dt = ∂ρ/∂t + (v . ∇)ρ = 0
بسیاری از فرمول های فیزیک از قانون بقای جرم سرچشمه می گیرند؛
اما همه این فرمول ها و به طور کلی تعریف این قانون، مربوط به فیزیک کلاسیک یا نیوتنی است.
در ادامه مقاله به فیزیک جدید هم اشاره می کنیم.
2# اثبات درستی قانون بقای جرم
اکثر عناصر از واکنش های همجوشی (fusion reactions) در ستاره ها یا ابر نواخترها تولید می شوند؛
بنابراین منطقی است که نباید در اثر یک واکنش شیمیایی از بین بروند یا تولید شوند.
گویا اتم هایی که اطرافمان می بینیم بسیار کهن سال هستند و البته می دانیم که
تعداد محدودی عنصر در طبیعت وجود دارند که پایه تمام اجزای جهان اطراف ما هستند.
یکی از بهترین روش های تحقیق درستی قانون بقای جرم این است که آزمایش ساده ای برای خود طراحی کنید.
یک قرص آلکا سلتزر (Alka seltzer- به عنوان مسکن استفاده می شود و داروی ضد اسید معده است)، مقداری آب و یک پاکت پلاستیکی قفل دار آماده کنید.
همه را با یک ترازوی گرمی وزن کنید.
آب و قرص را درون پلاستیک بریزید و بلافاصله در آن را ببندید.
پس از انجام آزمایش پاکت حاوی فرآورده ها را وزن کنید تا قانون بقای جرم را به عینه مشاهده کنید (وقتی قرص را در آب می ریزید، طی واکنش شیمیایی گازی آزاد می شود که درون پاکت گرفتار می شود).

3# اصلاح و نقض قانون بقای جرم
قانون بقای جرم بعداً توسط انیشتین در قانون حفظ انرژی و جرم اصلاح شد که
این واقعیت را توصیف می کند که کل جرم و انرژی در یک سیستم ثابت می ماند.
این اصلاحیه شامل این واقعیت است که جرم و انرژی می توانند به یکدیگر تبدیل شوند.
با این حال، قانون حفظ جرم همچنان یک مفهوم مفید در علم شیمی است؛
زیرا انرژی تولید شده یا مصرف شده در یک واکنش شیمیایی معمولی، مقدار کمی از جرم را تشکیل می دهد؛
بنابراین برای واکنش هایی با تبادل انرژی کم این قانون صادق است.
اما آیا جایی هست که این قانون به کلی نقض شود؟
پیش از این درباره تولید اتم ها از واکنش های همجوشی صحبت کردیم.
این یک نمونه از نقض پایستگی جرم است.
به طور کلی، مهم ترین جایی که در آن قانون پایستگی جرم نقض می شود، در واکنش های هسته ای است.
انرژی تبادل شده در این واکنش ها بسیار زیاد و غیر قابل چشم پوشی است.
در واکنش های شکافت هسته ای (تقسیم یک هسته سنگین به دو هسته با جرم کمتر) جرم محصولات شکافت، کمتر از جرم هسته مرکب است.
جرم کاسته شده تبدیل به انرژی می شود که مقدار این انرژی هم از ربطه زیر محاسبه می شود:
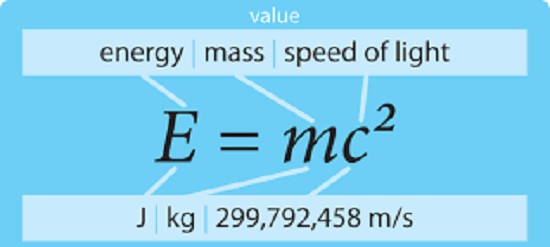
انرژی آزاد شده در هر واکنش شکافت، حدودا 108 برابر انرژی آزاد شده به ازای هر مولکول در یک واکنش معمولی مثل سوختن است.
احتمالا اکنون درک درستی از زیاد بودن انرژی دارید!
 |
نظرتون درباره این مقاله چیه؟
ما رو راهنمایی کنید تا اون رو کامل تر کنیم و نواقصش رو رفع کنیم.
توی بخش دیدگاه ها منتظر پیشنهادهای فوق العاده شما هستیم.


