با شنیدن نام هیدروکسید اولین چیزی که به ذهن شما می رسد چیست؟
سنگ ها و کانی های معدنی، شوینده های ضد عفونی کننده یا سود سوزآور؟
درست حدس زده اید، هیدروکسید در ساختار تمامی این ترکیبات وجود دارد.
در این مطلب برای شما خواهیم گفت که هیدروکسید چیست و چه کاربردهایی دارد.
با ما همراه باشید.
1# هیدروکسید چیست؟
–OH یک آنیون دو اتمی با نام شیمیایی هیدروکسید (Hydroxide) است.
هیدروکسید نام های دیگری مانند رادیکال هیدروکسیل، هیدروکسیل یا یون هیدروکسید نیز دارد.
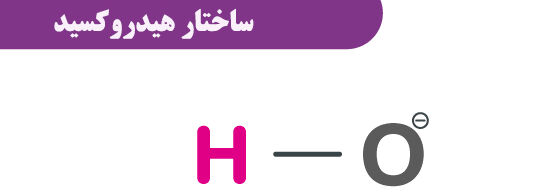
هیدروکسید از یک اتم هیدروژن و یک اتم اکسیژن تشکیل شده است که
با یک پیوند کووالانسی در کنار هم قرار گرفته اند.

هیدروکسید بار الکتریکی منفی دارد.
یون هیدروکسید کاربردهای گسترده ای دارد و نقش های مختلف آن عبارت اند از:
- نگهدارنده مواد غذایی
- قلیایی کننده ادرار برای جلوگیری از سنگ کلیه
- ضد انعقاد خون ذخیره شده
- بافر (buffer: محلولی بر پایه آب که در برابر تغییر pH ناشی از اضافه شدن کمی اسید یا باز مقاومت می کند و pH محلول را در محدوده مشخصی ثابت نگه می دارد)
- لیگاند (ligand: مولکول یا یونی است که با فلز پیوند برقرار کرده و ترکیب کمپلکس ایجاد می کند)
- کاتالیزور
- باز
- هسته دوست (nucleophile: یک اتم یا مولکول که یک جفت الکترون را برای ایجاد پیوند کووالانسی اهدا می کند)
2# خواص هیدروکسید
یون هیدروکسید نمک تشکیل می دهد.
برخی از این نمک ها در محلول آبی تجزیه می شوند و یون های هیدروکسید را در آب آزاد می کنند.
هنگامی که یک ماده الکتروپازتیو (electropositive) و هیدروکسید به یکدیگر متصل می شوند،
هیدروکسید یونیزه می شود، یک کاتیون هیدروژن آزاد و ترکیب اصلی را به اسید تبدیل می کند.

برای تکمیل پاسخ سوال هیدروکسید چیست، لازم است که
با خواص فیزیکی آن هم آشنا شویم که در جدول زیر به آن ها اشاره شده است:
| نام آیوپاک (IUPAC) | هیدروکسید |
| فرمول شیمیایی هیدروکسید | –OH |
| وزن مولکولی هیدروکسید | 17.007 گرم بر مول |
| جرم تک ایزوتوپی هیدروکسید | 17.003 گرم بر مول |
3# روش تشکیل هیدروکسید چیست؟
آیا می دانید روش تشکیل هیدروکسید چیست؟
رایج ترین روش تشکیل هیدروکسید، واکنش هیدراتاسیون چند فلز قلیایی و قلیایی خاکی کمیاب است.
به عنوان مثال، برای به دست آوردن هیدروکسید سدیم، باید سدیم فلزی را به آب اضافه کنیم که
از نظر شیمیایی به صورت زیر نشان داده می شود:
2Na + 2H2O → 2NaOH + H2

برای به دست آوردن هیدروکسید فلزاتی که مستقیماً با آب واکنش نمی دهند،
یک واکنش تبادلی یا متاتز (metathesis) انجام می شود که معمولا به صورت زیر است:
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
4# ظرفیت هیدروکسید چقدر است؟
یون هیدروکسید از دو اتم هیدروژن و اکسیژن ساخته شده است.
اکسیژن نسبت به هیدروژن اتم الکترونگاتیوتری است؛
بنابراین، اتم اکسیژن حامل 2 بار منفی است؛
در حالی که اتم هیدروژن حامل 1 بار مثبت است؛ بنابراین، OH بار کلی 1- دارد.
5# کاربردهای هیدروکسید چیست؟
- تولید پیل های سوختی
- تولید مواد ضد عفونی کننده
- نگهدارنده مواد غذایی برای جلوگیری از رشد باکتری ها و کپک ها در غذا
- استفاده از محلول های هیدروکسید سدیم یا به عبارتی کاستیک سودا (caustic soda) و سود سوزآور در ساخت خمیر و بازیافت کاغذ، تهیه انواع منسوجات، آب آشامیدنی، صابون ها، مواد شوینده و همچنین به عنوان پاک کننده فاضلاب
- بوکسیت، هیدروکسید آلومینیوم به عنوان سنگ معدن اصلی استخراج آلومینیوم
- استفاده از لپیدوکروسیت (γ-FeO(OH)) و گوتیت (α-FeO(OH)) برای استخراج آهن
- به عنوان پذیرنده پروتون در بازها (برای تشکیل آب، پروتون یا یون هیدروژن را از اسیدها دریافت می کنند. این معادله ساده ترین راه برای نشان دادن یک واکنش خنثی سازی است که می تواند به صورت H+ + OH– → H2O نشان داده شود)
- حضور رادیکال های هیدروکسید در ترکیبات آلی مانند قندها (فروکتوز، گلوکز، نشاسته و غیره)، صابون و لیپیدها (چربی ها)
- استفاده از چند هیدروکسید مانند آهک Ca(OH)2، برای تهیه کربنات کلسیم (CaCO3) و آمونیاک
- تصفیه هوا از طریق جذب گازهای اسیدی مانند دی اکسید کربن و دی اکسید گوگرد

6# سوالات متداول درباره هیدروکسید
- عدد pH هیدروکسید چیست؟
اگر pH محلولی کمتر از 7 باشد، محلول اسیدی، اگر تقریبا 7 باشد، محلول خنثی و اگر بیشتر از 7 باشد، محلول قلیایی در نظر گرفته می شود.
بنابراین، اگر در محلولی غلظت یون هیدروژن بیشتر از غلظت یون هیدروکسید باشد، محلول اسیدی است؛
اما اگر غلظت یون هیدروژن کمتر از غلظت یون هیدروکسید باشد، محلول قلیایی است.
اغلب محلول های هیدروکسیدی قلیایی هستند.
- آیا هیدروکسید به تنهایی وجود دارد؟
هیدروکسید زمانی که در آب است، به تنهایی وجود دارد؛
زیرا اسیدها و بازها یکدیگر را در محلول خنثی می کنند.
- آیا هیدروکسید خطرناک است؟
محلول های حاوی هیدروکسید به شدت خورنده هستند.
هیدروکسید سدیم بی بو است؛ بنابراین، بو عامل تشخیص این محلول های خطرناک نیست.
هیدروکسید سدیم مسمومیت گوارشی در بدن ایجاد نمی کند؛
اما باعث سوختگی شدید در تمام بافت هایی می شود که با آن تماس پیدا می کند.
 |
نظرتون درباره این مقاله چیه؟
ما رو راهنمایی کنید تا اون رو کامل تر کنیم و نواقصش رو رفع کنیم.
توی بخش دیدگاه ها منتظر پیشنهادهای فوق العاده شما هستیم.




خیلی عالی و کاربردی…مخصوصا این که میشه این مطالب ارزشمند رو به صورت فایل پی دی اف دانلود کرد. با تشکر
سلام جناب علیپور گرامی
ممنون از همراهی و حسن توجه شما
خوشحالیم که محتوا براتون مفید واقع شده، هدف ما در نماتک همین موضوع هست.
براتون آرزوی موفقیت داریم